Радиоактивность
Явление радиоактивности (от слова «радиус» — «луч»), или спонтанного
распада ядер, было открыто французским физиком Анри Беккерелем
(1852—1908) в 1896 году благодаря случайности. Он обнаружил, что уран
и его соединения испускают лучи или частицы, проникающие сквозь
непрозрачные тела и способные засвечивать фотопластинку. Беккерель
установил, что интенсивность излучения пропорциональна только
концентрации урана и не зависит от внешних условий (температура,
давление) и от того, находится ли уран в каких-либо химических
соединениях.
В 1897 году исследованиями урановых лучей занялись супруги Кюри —
Мария Склодовская-Кюри (1867-1934)и
Пьер Кюри (1859-1906).
Они доказали, что радиоактивные излучения испускаются не только атомами
урана, но и атомами некоторых других элементов. По радиоактивному
излучению ими были открыты два неизвестных ранее химических элемента
— радий и полоний.
Английскими физиками Эрнестом Резерфордом (1871—1937) и
Фредериком Содди (1877—1956) было доказано, что во всех радиоактивных
процессах происходят взаимные превращения атомных ядер химических
элементов. Изучение свойств излучения, сопровождающего эти процессы в
магнитном и электрическом полях, показало, что оно разделяется на
ci-частицы (ядра гелия), Р-частицы (электроны) и у-лучи
(электромагнитное излучение с очень малой длиной волны).
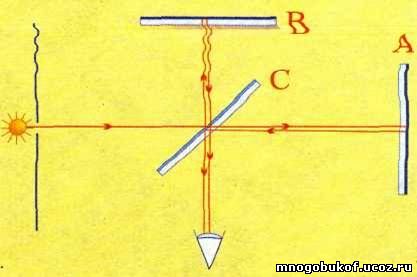
Используя прибор такого типа с альфа-частицами, испускаемыми
радием, Э. Резерфорд установил, что, хотя основная часть частиц
проходит сквозь золотую фольгу, на большие углы рассеивается больше
частиц, чем должно быть в соответствии с томсо-новской моделью атома.
Это было истолковано как указание на то, что в центре атома находится
малое ядро: 1 — радий, 2 — золотая фольга, 3 — экран из сульфида цинка,
4 — пучок И -частиц, 5 — рассеянные О- -частицы (малое число).
Исследуя явление рассеяния быстрых заряженных частиц при
прохождении через тонкие слои вещества, Резерфорд добился большого
прогресса в изучении структуры атомов. В этих опытах узкий пучок (X
-частиц, испускаемых радиоактивным веществом, направлялся на тонкую
металлическую пластинку. За пластиной помещался экран, покрытый слоем
кристаллов сульфида цинка, способных светиться под ударами быстрых
заряженных частиц. Резерфорд обнаружил, что большинство <Х -частиц
отклоняется от прямолинейного пути на углы не более 1—2°. Однако
небольшая доля & -частиц испытывала отклонение на значительно
большие углы. Это явление Резерфорд объяснил тем, что положительный
заряд в атоме не распределен равномерно в шаре радиусом 10~10 м, как в
модели Томсона,
а сосредоточен в центральной части атома в области значительно меньших
размеров. В этой центральной положительно заряженной части атома —
атомном ядре — сосредоточена почти вся масса атома. Расчеты Резерфорда
показали, что радиус атомного ядра равен примерно 10~15 м. Резерфорд
предположил, что атом устроен подобно планетной системе. Как вокруг
Солнца на больших расстояниях от него обращаются планеты, так электроны
в атоме обращаются вокруг атомного ядра. Радиус круговой орбиты самого
далекого от ядра электрона и есть радиус атома. Такая модель атома
была названа «планетарной» моделью. Вскоре после появления
«планетарной» модели атома было обнаружено, что от количества
электронов зависят химические свойства элемента. Наши сегодняшние
знания позволяют составить периодическую таблицу элементов,
последовательно добавляя протоны к ядру самого легкого атома,
состоящего из одного протона и одного электрона — атома водорода, а
также соответствующее число электронов к «оболочке» атома.
Взаимодействие между атомами порождает различные химические процессы,
так что вся химия может быть понята на основе законов атомной физики.
Однако, согласно электродинамике Максвелла, такой атом не может быть
устойчивым: двигаясь по круговым (или эллиптическим) орбитам, электрон
испытывает ускорение, а поэтому он должен излучать электромагнитные
волны с частотой, равной частоте его обращения вокруг ядра. Это, в
свою очередь, будет приводить к уменьшению энергии.
Потеря энергии приведет электрон к падению на ядро. Таким образом,
подобный атом не может существовать в реальности. Разработка следующей
модели атома принадлежит
Нильсу Бору (1885—1962).
Взяв за основу модель Резерфорда, он использовал и идеи квантовой
теории. Свои представления о структуре атома Бор сформулировал в виде
следующих
постулатов.









 flamer87@mail.ru
flamer87@mail.ru
 314713830391
314713830391
 SiMARkL@qip.ru
SiMARkL@qip.ru
 595440134
595440134